Luigi Ricciardi 1 , Rosa Mazzeo 2,*© , Angelo Raffaele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1 © et Concetta Lotti 2,*
- 1 Département des sciences du sol, des plantes et de l'alimentation, Unité de génétique végétale et de sélection, Université de Bari, Via Amendola 165/A, 70125 Bari, Italie ; luigi.ricciardi@uniba.it (G / D);angelo.marcotrigiano@uniba.it (BRAS); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Département des Sciences de l'Agriculture, de l'Alimentation et de l'Environnement, Université de Foggia, Via Napoli 25, 71122 Foggia, Italie
- 3 Département des biosciences, biotechnologies et biopharmaceutiques, Université de Bari, Via Orabona 4, 70125 Bari, Italie ; guglielmo.rainaldi@uniba.it
- 4 Département des technologies énergétiques, Division de la bioénergie, de la bioraffinerie et de la chimie verte, Centre de recherche ENEA Trisaia, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italie ; paolo.iovieno@enea.it
* Correspondance: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Résumé:
d'oignon (Allium cepa L.) est la deuxième culture maraîchère la plus importante au monde et est largement appréciée pour ses bienfaits pour la santé. Malgré son importance économique significative et sa valeur en tant qu’aliment fonctionnel, l’oignon a été peu étudié en ce qui concerne sa diversité génétique. Nous avons étudié ici la variation génétique de «l'oignon rouge Acquaviva» (ARO), une variété locale cultivée depuis un siècle dans une petite ville de la province de Bari (Pouilles, sud de l'Italie). Un ensemble de 11 marqueurs microsatellites a été utilisé pour explorer la variation génétique dans une collection de matériel génétique composée de 13 populations d'ARO et de trois types commerciaux courants. Les analyses de la structure génétique avec des méthodes paramétriques et non paramétriques ont mis en évidence que l'ARO représente un pool génétique bien défini, clairement distinct des races locales Tropea et Montoro avec lesquelles il est souvent confondu. Afin de fournir une description des bulbes, habituellement utilisés pour la consommation fraîche, la teneur en solides solubles et le piquant ont été évalués, montrant une douceur plus élevée dans l'ARO par rapport aux deux variétés locales mentionnées ci-dessus. Dans l'ensemble, la présente étude est utile pour la valorisation future de l'ARO, qui pourrait être promue à travers des labels de qualité qui pourraient contribuer à limiter les fraudes commerciales et à améliorer les revenus des petits exploitants.
Introduction
Le genre Allium comprend environ 750 espèces [1], parmi lesquelles l'oignon (Allium cepa L., 2n = 2x =16) est l'une des plus répandues. A. cepa a un cycle biennal et un comportement reproducteur croisé. Aujourd’hui, la production mondiale d’oignon (97.9 Mt) en fait la deuxième culture légumière après la tomate [2]. Depuis l’Antiquité, les bulbes d’oignons sont utilisés à la fois comme aliment et dans des applications médicinales traditionnelles. En effet, les anciens Egyptiens rapportaient déjà plusieurs formules thérapeutiques basées sur l'utilisation de l'ail et des oignons dans un papyrus médical de 1550 avant JC, le Codex Ebers [3].
Ce légume polyvalent et sain est consommé cru, frais ou transformé, et utilisé pour rehausser le goût de nombreux plats. Plusieurs études récentes affirment que la consommation d'oignons peut réduire le risque de maladies cardiovasculaires [4,5], d'obésité [6], de diabète [7] et de diverses formes de cancer [8-10]. Les propriétés bénéfiques de l'oignon pour la santé sont souvent attribuées à des niveaux élevés de deux classes de composés nutraceutiques : les flavonoïdes et les sulfoxydes d'alk(én)ylcystéine (ACSO). La première classe comprend les flavonols et les anthocyanes. La quercétine est le principal flavonol détectable, connu pour ses fortes propriétés antioxydantes et anti-inflammatoires dans l'élimination des radicaux libres et la liaison des ions de métaux de transition. ; tandis que les anthocyanes confèrent une couleur rouge/violette à certaines variétés d'oignons. Quant aux ACSO, le plus abondant est l'isoalliine [(+)-trans-S-1-propényl-L-cystéine sulfoxyde] , un acide aminé soufré non volatil et non protéinogène stocké dans les cellules, qui est indirectement responsable de l'arôme et du goût piquants des oignons . Lors de la rupture des tissus, l'isoalliine est clivée par l'enzyme alliinase pour produire une série de composés volatils (pyruvate, ammoniac, thiosulfonates et S-oxyde propanethial) qui provoquent un larmoiement et provoquent une odeur désagréable (piquante). . Le piquant de l'oignon est souvent mesuré comme la quantité, par gramme de poids frais, d'acide pyruvique généré par l'hydrolyse. [15,16].
Dans les pays du bassin méditerranéen, proposé comme l'un des centres secondaires de diversité de A. cepa [17,18], les bulbes d'oignon présentent une grande variabilité en termes de forme, de taille, de couleur, de matière sèche et de piquant. [19-dix]. De plus, la fertilisation à base de soufre, les pratiques agronomiques, le type de sol, les conditions climatiques et le génotype des cultivars ou des races locales peuvent influencer la qualité du bulbe en lui conférant des valeurs organoleptiques et nutritionnelles particulières. [23-dix]. En Italie, malgré la grande disponibilité de matériel génétique d'oignon, seules quelques variétés d'oignons sont souvent soumises à des études scientifiques et correctement caractérisées. [28,29].
Une caractérisation génétique et phénotypique approfondie de l'agrobiodiversité est cruciale pour assurer une conservation appropriée des ressources phytogénétiques et promouvoir l'utilisation de génotypes spécifiques dans la chaîne de valeur. [30-dix]. Les marqueurs de répétition de séquence simple (SSR) ont souvent été choisis pour la cartographie [33-dix], empreintes génétiques et discrimination des cultivars [36-dix]et estimation fiable de la variabilité génétique au sein et entre les races locales [39-dix], car ils sont spécifiques à un locus, multi-alléliques, hérités de manière codominante, hautement reproductibles et adaptés au génotypage automatisé.
Dans la présente étude, nous avons concentré notre attention sur une variété locale traditionnelle des Pouilles, l'« oignon rouge Acquaviva » (ARO), cultivé selon des méthodes d'agriculture biologique dans une petite zone de la ville d'Acquaviva delle Fonti, dans la province de Bari. (Pouilles, Italie du Sud). Les bulbes de cette variété locale sont gros, aplatis et de couleur rouge et sont largement utilisés dans les recettes locales. Bien que l'ARO ait obtenu le label de qualité « Slow Food Presidium », sa production pourrait être davantage encouragée et protégée par des labels de qualité de l'Union européenne tels que l'indication géographique protégée (IGP) et l'appellation d'origine protégée (OPD), car ceux-ci pourraient contribuer à limiter la fraudes commerciales et améliorer les revenus des petits exploitants. Ici, les marqueurs moléculaires SSR ont été utilisés comme outils puissants pour évaluer la variation génétique parmi les populations d'ARO et pour discriminer cette race locale des deux autres races locales d'oignons rouges du sud de l'Italie. De plus, nous avons estimé le piquant et la teneur en solides solubles afin d'évaluer la saveur ARO en relation avec la demande du marché.
Résultats
Création de la collection de matériel génétique d'oignon rouge Acquaviva et caractérisation morphologique
Les graines de 13 populations de la race locale ARO, données par les agriculteurs dans le cadre du projet BiodiverSO Région des Pouilles, ont été utilisées pour établir une collection de matériel génétique ARO.
Des descripteurs morphologiques, liés au bulbe, à la peau et à la chair, ont été collectés sur le matériel génétique ARO et sur trois variétés locales d'oignons, deux appartenant à la race locale « oignon rouge Tropea » (TRO) et un à la race locale « oignon cuivré Montoro » (MCO) (Figure 1). Tous les bulbes ARO étaient plats et caractérisés par une peau externe et une chair rouges avec différentes nuances de rouge. En revanche, la chair des bulbes TRO était entièrement rouge, alors que celle des bulbes MCO était peu pigmentée (tableau S1). L'analyse biochimique a permis d'évaluer la teneur en solides solubles et le piquant. Comme indiqué dans le tableau 1, les valeurs moyennes de la teneur en matières solides solubles des bulbes dans les populations ARO étaient de 7.60 et variaient de 6.00 (ARO12) à 9.50° Brix (ARO11 et ARO13). Cette valeur était supérieure à celle estimée pour les variétés locales TRO et MCO (respectivement 4.25 et 6.00° Brix).

Tableau 1. Contenu solide soluble et valeurs de piquant évalués dans les populations d'« oignon rouge Acquaviva » (ARO), « oignon rouge Tropea » (TRO) et « oignon cuivre Montoro » (MCO) *.
| CODE | Contenu solide soluble (Brix) | Piquant (pmolg-1 FW) | ||
| Médian | CV y (%) | Médian | CV y (%) | |
| ARO1 | 6.25 J* | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 à | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28 ab | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 à | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 à | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 ab | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 ab | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 à | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 à | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 ab | 6.57 |
| ARO11 | A 9.50 | 7.44 | 5.54 ab | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 ab | 9.70 |
| ARO13 | A 9.50 | 7.44 | 6.63 à | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 ab | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 ab | 4.79 |
* Les moyennes avec les mêmes lettres en majuscules ou en minuscules ne sont pas statistiquement différentes à 0.01P ou 0.05P, respectivement (test de SNK). y Coefficient de variation.
La valeur moyenne du piquant de l'ARO, évaluée au moyen de la teneur en acide pyruvique, était de 6.00, variait de 4.51 pmol g-1 FW (ARO6) à 7.04 (ARO8). Cette valeur était supérieure à celle estimée dans les variétés locales TRO et MCO (3.54 pmol g-1 FW et 4.18 pmol g-1 FW, respectivement).
Polymorphisme SSR et relations génétiques entre les accessions
Dans la présente étude, 11 des 37 combinaisons d'amorces SSR testées ont fourni des polymorphismes à locus unique, c'est-à-dire donnant au plus deux produits d'amplification chez un seul individu. Au total, 55 allèles ont été détectés chez 320 individus avec un nombre d'allèles par locus allant de 2 (ACM147 et ACM 504) à 11 (ACM132) et une valeur moyenne de 5 allèles (Tableau 2). Dans les populations individuelles, le nombre d'allèles (Na) variait de 1.94 (ACM147 et ACM504) à 5.38 (ACM132), tandis que le nombre effectif d'allèles (Ne) variait de 1.41 (ACM152) à 2.82 (ACM449). Écarts entre les valeurs de Na et Ne étaient dues à la présence d'allèles peu fréquents dans les populations et à la prédominance de quelques allèles seulement. La valeur d'hétérozygotie (Ho) la plus élevée observée a été mise en évidence pour ACM138 et ACM449 (0.62), tandis que la plus faible était associée à ACM152 (0.25). L'hétérozygotie attendue (He), qui correspond à l'attente théorique dans une population panmictique, variait de 0.37 (ACM504) à 0.61 (ACM132, ACM138 et ACM449). L'indice de fixation de Wright (Fis) affichait des valeurs proches de zéro (moyenne 0.05) pour tous les marqueurs, indiquant des valeurs similaires entre les niveaux d'hétérozygotie observés et attendus, comme prévu pour une espèce croisée. L'efficacité du marqueur SSR individuel dans l'empreinte génétique a été estimée par l'indice de contenu d'information polymorphe (PIC), avec une valeur moyenne de 0.48 et variait de 0.33 (ACM504) à 0.67 (ACM132). Un autre indice d'efficacité, l'indice d'information de Shannon (I), affichait une valeur moyenne de 0.84 et des valeurs supposées comprises entre 0.45 (ACM152) et 1.20 (ACM132).
Tableau 2. Caractéristiques du polymorphisme des 11 marqueurs SSR utilisés pour estimer la diversité génétique dans les populations ARO, TRO et MCO. Le nombre total d'allèles (Na), la plage de tailles de bande et l'indice de contenu d'informations polymorphes (PIC) se réfèrent à l'ensemble total de 320 individus génotypés dans cette étude. Nombre d'allèles (Na), nombre d'allèles effectifs (Ne), hétérozygotie observée (Ho), hétérozygotie attendue (He), indice de fixation (Fis), et l'indice d'information de Shannon (I) font référence aux valeurs moyennes calculées à partir de 16 populations, chacune composée de 20 individus.
| Lieu. | Na total | Plage de taille (pb) | PIC | Médian | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | - 0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | - 0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | - 0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | - 0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Médian | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Parmi les populations, ARO3, ARO6, ARO8, ARO10, TRO1 et MCO présentaient un niveau élevé de variation génétique (Ho > 0.5), alors que la diversité la plus faible a été observée dans la population ARO7 (Ho = 0.27) (Tableau supplémentaire S2). Dans l'ensemble, toutes les accessions affichées Fis valeurs proches de zéro (Fis valeur moyenne = 0.054), comme prévu dans des conditions d'accouplement aléatoires.
Analyse de la variance moléculaire et de la structure génétique
La répartition hiérarchique de la variation génétique entre et au sein des populations a été calculée par AMOVA. Les résultats ont mis en évidence une fraction considérable de variation génétique au sein des populations (87 %). La variation entre les populations, 13 %, était très significative (P < 0.001) (Tableau 3). Les valeurs par paires du paramètre Fpt, analogue à l'indice de fixation Fst de Wright, allant de 0.002 (ARO2/ARO10) à 0.468 (ARO7/TRO2), étaient significatives (P <0.05), à l'exception de neuf comparaisons par paires (tableau supplémentaire S3).
Tableau 3. Analyse de la variance moléculaire de 320 génotypes provenant de 16 populations de Allium cepa L.
| Identifier | df | Somme des carrés | Estimation de l'écart | Écart (%) | Fpt | P |
| Parmi les populations | 15 | 458.63 | 1.16 | 13% | ||
| Au sein des populations | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Total | 319 | 2731.62 | 8.66 |
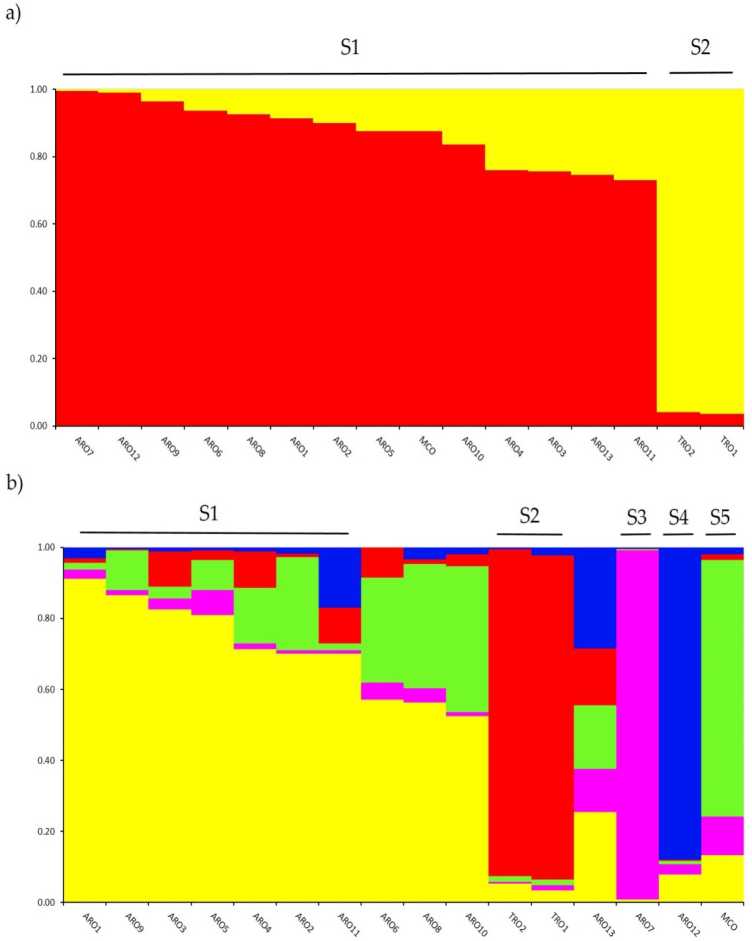
Étude de la structure génétique chez A. cepa La collection génotypée dans cette étude a été réalisée au moyen de l'analyse de regroupement basée sur un modèle de mélange mise en œuvre dans le logiciel STRUCTURE. La méthode Evanno AK a suggéré la subdivision en deux groupes (K = 2) comme la plus informative pour notre jeu de données,avec Ee next pe le plus élevéok à K = 5 (figure supplémentaire S1). A fourchette = 2, ahpopulations wavant le culigned aussineof les deux clusters comprenant un coefficient de rnernbertoip (q) > 0.7. Comme shoje suis dans Figure 2a, le premier cluster (nommé S1) comprenait MCO et toutes les populations ARO, tandis que le cluster S2 regroupait les deux populations TRO. À K = 5, fournissant une description plus approfondie de l'ensemble de données (Figure 2b), 75% des accessions ont été attribuées à l'un des cinq clusters. La séparation entre ARO (S1) et TRO (S2) a été confirmée, bien que certaines populations d'ARO aient été mélangées (q <0.7, 3) ou regroupées séparément dans les deux nouveaux groupes S4 et S7 (ARO12 et ARO5, respectivement). Il est intéressant de noter que le type commercial MCO formait une grappe distincte (SXNUMX) séparée de l’oignon rouge des Pouilles.
Relations génétiques entre les populations
Le polymorphisme SSR a permis de tracer un dendrogramme de la diversité génétique et les résultats de l'analyse phylogénétique sont présentés dans la figure 3a. Ici, la collection de matériel génétique a été divisée en cinq groupes fortement soutenus par des valeurs bootstrap. Les populations ARO7 et ARO12 ont été immédiatement séparées des populations restantes et ont formé deux groupes distincts. Le troisième cluster comprenait les deux populations commerciales de TRO, tandis que le quatrième nœud divisait MCO de onze populations ARO. Les relations génétiques existant entre les populations ont été étudiées plus en détail au moyen d'une analyse des coordonnées principales (PCoA) (Figure 3b). Comme souligné précédemment, les populations d'ARO étaient étroitement regroupées, à l'exception d'ARO12 et d'ARO7, qui apparaissaient dans des positions isolées dans le graphique PCoA. Les deux populations TRO et MCO étaient dispersées dans le panneau inférieur droit du graphique.
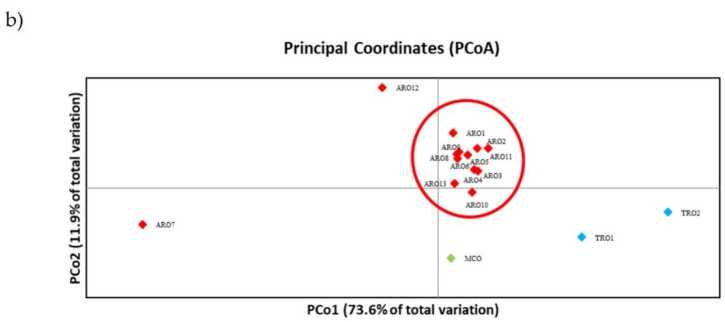
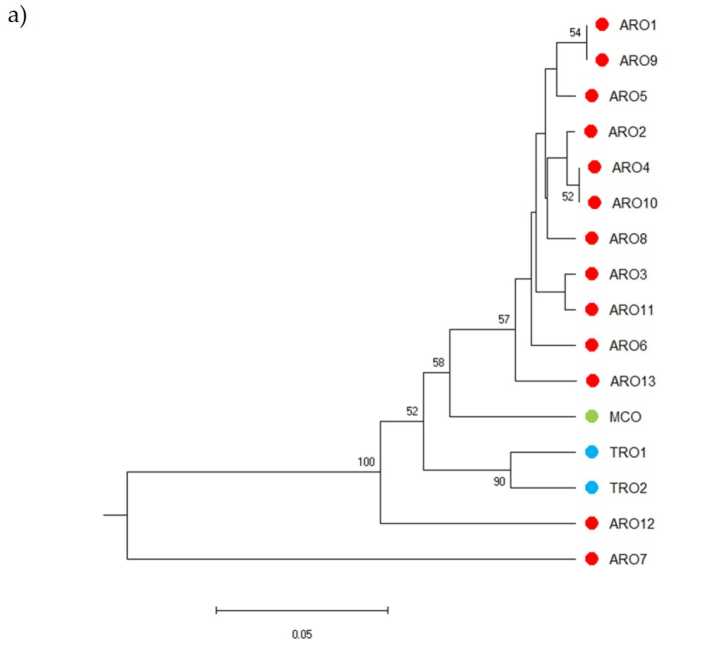
Figure 3. Diversité génétique parmi 16 A. cepa populations caractérisées dans cette étude, en fonction de leur profil SSR. (a) Dendrogramme UPGMA de distance génétique. Les valeurs de prise en charge du bootstrap > 50 sont indiquées au-dessus des nœuds correspondants ; (b) analyse en composantes principales (PCoA). Le cluster entouré en rouge correspond parfaitement au groupe généré par l'analyse phylogénétique et constitué de 11 accessions ARO.
a lieu
Au sein de la grande biodiversité agricole traditionnellement cultivée dans le sud de l’Italie, les variétés locales d’oignons représentent des produits de niche qui doivent être préservés du risque d’érosion génétique et de la menace de remplacement par des cultivars modernes. Dans le cadre du projet régional BiodiverSO, visant à collecter, caractériser, promouvoir et sauvegarder les ressources génétiques de la région des Pouilles fortement liées au patrimoine local, nous avons établi une collection de graines de 13 populations de la race locale ARO. Nous avons rapporté la première évaluation de la variation de l'ARO en termes de polymorphismes de l'ADN et de deux paramètres biochimiques, la teneur en solides solubles et en acide pyruvique, liés aux traits aromatiques et importants pour l'acceptation des produits frais non cuits. De plus, les données sur la race locale ARO ont été comparées à celles recueillies sur deux autres races locales d'oignons pigmentés avec lesquelles elle est souvent confondue.
Les analyses biochimiques ont mis en évidence le goût sucré des 13 populations d'ARO, lié à une teneur élevée en solides solubles et un piquant moyen, selon les directives de l'industrie de l'oignon doux. . Les bulbes ARO étaient plus sucrés que ceux des variétés locales TRO et MCO et affichaient un piquant légèrement plus élevé. Cependant, le goût sucré des oignons est dû à un équilibre entre la teneur en sucre et le piquant, cette caractérisation pourrait donc être utile pour soutenir la sélection de génotypes de valeur, généralement effectuée par les agriculteurs uniquement sur la base de la morphologie.
Les marqueurs SSR se sont avérés être un outil utile pour discriminer les génotypes, bien que collectés dans une zone de culture étroite telle que la ville d'Acquaviva delle Fonti. Les marqueurs sélectionnés affichaient un nombre d'allèles plus élevé que les marqueurs précédemment rapportés par ainsi que le , mais inférieur aux marqueurs rapportés par . De plus, 50 % de notre ensemble de marqueurs présentaient des valeurs d'indice PIC supérieures à 0.5, ce qui s'avère approprié pour discriminer les populations de la collection, comme le suggère . L'évaluation de la diversité au sein des populations a révélé des valeurs similaires entre Ho et He, entraînant un faible Fis valeurs. Ceci est en accord avec la nature croisée de A. cepa, qui souffre sérieusement de dépression de consanguinité . Le Fi globals la valeur calculée dans les populations d'oignons considérées dans cette étude (0.054) était inférieure à celle rapportée précédemment par (0.22) et presque identique à celui trouvé par de Géographie (0.08) et avec la (0.00) qui ont évalué la diversité génétique des variétés locales d'oignons du nord-ouest de l'Espagne et du Niger, respectivement. Des niveaux remarquables d'hétérozygotie dans les populations d'ARO renforcent l'idée selon laquelle les Pouilles représentent un centre de diversité pour de nombreuses espèces horticoles. [32, 42, 49-dix].
AMOVA a souligné que la plupart des variations moléculaires dans la collection génotypée dans cette étude se situent au sein des populations. Cependant, une différenciation génétique significative entre les populations (FPT valeurs) ont révélé l’apparition d’une stratification génétique. En fait, bien que nos résultats indiquent la présence d'une uniformité génétique dans la plupart des populations ARO, formant un groupe bien défini, les populations ARO7 et ARO12 présentaient un profil génétique clairement distinct. Ce résultat pourrait être dû à une origine différente des semences utilisées par les deux agriculteurs auprès desquels les populations ont été collectées. De plus, sur la base des résultats obtenus, la race locale ARO peut être considérée comme clairement distincte au niveau génétique des races locales TRO et MCO. Dans une étude récente, a évalué la diversité génétique de plusieurs variétés locales d'oignons italiens, notamment « Acquaviva », « Tropea » et « Montoro ». Bien que les auteurs aient utilisé des marqueurs SNP pour évaluer la diversité génétique d’une collection d’oignons plus large, le génotypage n’a pas permis de distinguer les oignons « Acquaviva » des oignons « Tropea » et « Montoro ». Cet écart est probablement dû à la faible valeur moyenne du PIC trouvée (0.292), ce qui suggère un caractère informatif général modeste des locus analysés, comme le prétend . De plus, afin d'étudier la présence de sous-structure dans leur cluster italien, il aurait été préférable d'analyser les génotypes italiens séparément du reste de la collection. Cela aurait probablement permis de visualiser un modèle de diversité génétique lié à la stratification géographique ou à des traits sous sélection empirique.
En conclusion, la présente étude représente un rapport complet sur une variété locale d'oignon associée au patrimoine culturel local et d'importance économique pour les agriculteurs. Nos résultats mettent en évidence que, à quelques exceptions près, l’ARO se caractérise par un pool génétique bien défini, qui mérite d’être préservé du risque d’érosion génétique. Par conséquent, la création d’une collection représentative de cette précieuse source de diversité génétique a été cruciale. Enfin, la caractérisation génétique et phénotypique des ORA pourrait être utile pour obtenir des labels de qualité de l'Union européenne.
Matériels et méthodes
Collecte de matériel génétique, matériel végétal et extraction d'ADN
Un ensemble de 13 populations de la race locale ARO ont été acquises dans le cadre d'un projet de la région des Pouilles (BiodiverSO : https://www.biodiversitapuglia.it/), à travers une série de missions réalisées à « Acquaviva delle Fonti », une petite ville des Pouilles dans la province de Bari, en Italie. Les sites de collecte de chaque accession ont été cartographiés via le système d'information géographique (SIG) et rapportés dans le tableau 4. De plus, deux populations de la race locale TRO et une population de la race locale MCO ont été incluses dans la présente étude et utilisées comme références. Tout le matériel végétal a été cultivé dans les mêmes conditions environnementales dans la ferme expérimentale « P Martucci » de l'Université de Bari (41° 1'22.08″ N, 16°54'25.95″ E), sous cage de protection pour éviter la pollinisation croisée entre populations et assurer la pollinisation intra-population au moyen de mouches à viande (Lucilia César). Les 16 populations ont été caractérisées pour des caractères liés à la taille et à la forme du bulbe, ainsi qu'à la couleur de la peau et de la chair (tableau S1). De plus, le contenu solide soluble a été analysé à l'aide d'un réfractomètre portatif et le piquant a été mesuré dans des échantillons de jus d'oignon en ajoutant de la 2,4-dinitrophényl hydrazine (0.125 % v/v dans 2N de HCl) et en évaluant l'absorbance à 420 nm, comme rapporté par . Le test multi-gammes de Duncan et le test SNK ont été réalisés pour déterminer la présence de différences significatives.
Tableau 4. Liste des populations collectées et génotypées dans cette étude. Pour chaque population, le code d'identification, le nom local, les coordonnées GPS et la banque de gènes préservant les graines sont indiqués.
| Code | Nom | Les coordonnées GPS | Banque de gènes y |
| ARO1 | Cipolla rouge d'Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rouge d'Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rouge d'Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rouge d'Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rouge d'Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rouge d'Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rouge d'Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rouge d'Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rouge d'Acquaviva | 40°54»51.372″ N16°49»3.504 » E | Di.SSPA |
| ARO10 | Cipolla rouge d'Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rouge d'Acquaviva | 40°52»49.8″ N16°49»48.575 » E | Di.SSPA |
| ARO12 | Cipolla rouge d'Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rouge d'Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa longa de Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MCO | Cipolla ramata de Montoro | - | Di.SSPA |
| y Di.SSPA, Département des Sciences des Sols, des Plantes et des Aliments, Université de Bari. |
Des feuilles de 20 génotypes par population ont été échantillonnées et conservées à -80 °C jusqu'à leur utilisation. Pour les espèces riches en polysaccharides, comme A. cepa, les premières étapes d'élimination du polysaccharide sont essentielles pour obtenir un ADN de bonne qualité, c'est pourquoi les lavages initiaux dans un tampon STE (saccharose 0.25 M, Tris 0.03 M, EDTA 0.05 M) ont été effectués comme décrit par . L'ADN total a été extrait selon la méthode CTAB et enfin, la qualité et la concentration ont été vérifiées par le spectrophotomètre UV-vis Nano Drop 2000 (ThermoScientific, Waltham, MA, USA) et par électrophorèse sur gel d'agarose à 0.8%.
Analyse RSS
16 combinaisons d'amorces EST-SSR développées par et déjà testé dans des études sur la diversité génétique par ainsi que le et 21 SSR génomiques [45-dix] ont été sélectionnés pour évaluer leur pertinence (tableau supplémentaire S4). Le génotypage a été réalisé à l'aide de la méthode économique de marquage fluorescent dans laquelle la queue M13 est ajoutée à chaque amorce SSR directe. . Les mélanges PCR ont été préparés dans 20 gL de réaction contenant : 50 ng d'ADN total, 0.2 mM de mélange dNTP, 1X de tampon de réaction PCR, 0.8 U d'ADN polymérase DreamTaq (Thermo Scientific, Waltham, MA, USA), 0.16 gM d'amorce inverse. , 0.032 gM d'amorce directe étendue avec la séquence M13 (5′-TGTAAAACGACGGCCAGT-3') et 0.08 gM d'amorce universelle M13 marquée avec des colorants fluorescents FAM ou NED (Sigma-Aldrich, St. Louis, MO, USA). Les réactions PCR ont été réalisées dans le thermocycleur SimpliAmp (Applied Biosystems, CA, USA) avec les conditions suivantes pour la majorité des paires d'amorces : 94 °C pendant 5 min, 40 cycles à 94 °C pendant 30 s, 58 °C. pendant 45 s et 72 °C pendant 45 s et un allongement final à 72 °C pendant 5 min. Quant aux ACM446 et ACM449, une PCR touchdown a été appliquée avec un recuit de 60 °C à 55 °C sur 10 cycles, 30 cycles à 55 °C, suivi d'une extension finale de 5 min à 72 °C. Les produits de PCR ont été chargés dans une plaque à 96 puits et mélangés avec 14 gL de Hi-Di Formamide (Life Technologies, Carlsbad, CA, USA) et 0.5 gL de GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, USA). Les amplicons ont été résolus au moyen de la machine de séquençage capillaire ABI PRISM 3100 Avant Genetic Analyser (Life Technologies, Carlsbad, CA, USA), où les allèles ont été notés comme codominants et attribués à l'aide du logiciel GeneMapper version 3.7.
Les logiciels GenAlEx 6.5 et Cervus 3.0.7 ont été utilisés pour estimer le nombre d'allèles (Na), le nombre d'allèles efficaces (Ne), l'hétérozygotie observée (Ho), l'hétérozygotie attendue (He), le contenu d'information polymorphe (PIC), l'indice d'information de Shannon (I) et l'indice de fixation (Fis ) pour chaque locus SSR.
Évaluation de la diversité génétique
Le partitionnement hiérarchique de la variation génétique parmi et au sein des populations d'oignons a été évalué par GenAlEx 6.5 grâce à l'analyse de la variance moléculaire (AMOVA) avec 999 bootstrapping pour tester la signification. De plus, le logiciel GenAlEx 6.5 a été utilisé pour estimer la diversité au sein de chaque population en calculant la moyenne de Ho, He et Fis sur tous les loci SSR.
La structure de la population a été déduite par l'algorithme de clustering basé sur un modèle bayésien implémenté dans le logiciel STRUCTURE v.2.3.4. . L'ensemble de données a été exécuté avec un certain nombre de groupes hypothétiques (K), allant de 1 à 10, en définissant dix exécutions indépendantes pour chaque valeur K. Pour chaque analyse, visant à vérifier la cohérence des résultats, 100,000 100,000 périodes de rodage initiales et XNUMX XNUMX itérations de chaîne de Markov Monte Carlo (MCMC) ont été réalisées sous le modèle de mélange et avec des fréquences d'allèles indépendantes parmi les populations. La valeur K la plus probable a été déterminée en mettant en œuvre la méthode AK, décrite par , dans le programme Web STRUCTURE HARVESTER . Une population individuelle a été affectée à un cluster spécifique lorsque son coefficient d'appartenance (valeur q) était supérieur à 0.7, XNUMX, sinon elle était considérée comme d'ascendance mixte.
Une analyse des coordonnées principales a été réalisée afin de visualiser les modèles de relations génétiques entre les accessions révélés par la matrice de distance génétique de Nei (tableau supplémentaire S5). Sur la base des fréquences alléliques, un dendrogramme de distance génétique a été construit en mettant en œuvre la méthode des groupes de paires non pondérés avec moyennes arithmétiques (UPGMA) dans le logiciel POPTREEW. . Le bootstrapping a été appliqué pour évaluer la confiance dans le clustering hiérarchique, en définissant 100 rééchantillonnages de l'ensemble de données. Enfin le logiciel MEGA X a été utilisé comme logiciel de dessin d’arbres.
Matériel supplémentaire : Les éléments suivants sont disponibles en ligne sur http://www.mdpi.com/2223-7747/9/2/260/s1. Tableau S1 : Caractérisation morphologique des bulbes ARO, MCO et TRO. Tableau S2 : Indices d'hétérozygotie et de fixation calculés pour les races locales ARO et les races locales TRO et MCO. Tableau S3 : Valeurs par paires du paramètre Fpt. Tableau S4 : Liste des SSR utilisés dans l'étude. Tableau S5. Matrice de population par paires de distance génétique Nei. Figure S1 : Graphique linéaire des valeurs K changeant avec le Delta K d'Evanno.
Contributions d'auteur: CL et LR ont conçu l'étude et conçu l'expérience ; CL et PI ont effectué une analyse des marqueurs moléculaires ; ARM et VZ ont réalisé les essais sur le terrain ; RM, SP, GR et CL ont participé à l'analyse des données ; RM et CL ont rédigé le manuscrit. Tous les auteurs ont lu et accepté la version publiée du manuscrit.
Financement: Ce travail a été financé par le projet régional des Pouilles « Biodiversité des espèces végétales des Pouilles » – Programma di Sviluppo Rurale per la Puglia 2014-2020. Misura 10—Sottomisura 10.2 ; subvention CUP H92C15000270002, Italie.
Remerciements: Nous remercions l'« Azienda Agricola Iannone Anna » et l'« Association produttori della vera cipolla rossa di Acquaviva » pour la fourniture du matériel végétal utilisé dans l'expérience.
Conflits d'intérêts: Les auteurs ne déclarent aucun conflit d'intérêt.
Bibliographie
- 1. Stearn, WT Combien d'espèces d'Allium sont connues ? Kew Mag. 1992, 9, 180-182. [CrossRef]
- 2. FAOSTAT. Base de données statistiques de la FAO. Disponible en ligne: http://www.fao.org/2017 (consulté sur 8 Janvier 2019).
- 3. Block, E. La chimie de l'ail et de l'oignon. Sci. Un m. 1985, 252, 114-119. [CrossRef]
- 4. Lee, B. ; Jung, JH; Kim, HS Évaluation de l'oignon rouge sur l'activité antioxydante chez le rat. Chimie alimentaire. Toxicol. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM ; Lune, J. ; Chung, JH; Cha, YJ; Shin, MJ Effet des extraits de pelure d'oignon riches en quercétine sur la thrombose artérielle chez le rat. Chimie alimentaire. Toxicol. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O. ; Shiojima, Y. ; Igarashi, K. Effets anti-obésité de l'extrait d'oignon chez les rats gras diabétiques Zucker. Nutriments 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH ; Rehman, K. ; Chen, S. Spice plant Allium cepa : Complément alimentaire pour le traitement du diabète sucré de type 2. Nutrition 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y. ; Tian, Wisconsin ; Ma, XF Effets inhibiteurs de l'oignon (Allium cepa L.) extrait sur la prolifération des cellules cancéreuses et des adipocytes via l'inhibition de la synthase des acides gras. Pac asiatique. J. Cancer Préc. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW ; Hsu, Caroline du Sud ; Chueh, FS ; Chen, YY; Yang, JS; Lin, JP ; Lien, JC; Tsai, CH ; Chung, JG La quercétine inhibe la migration et l'invasion des cellules cancéreuses buccales humaines SAS grâce à l'inhibition des voies de signalisation NF-kappaB et métalloprotéinase-2/-9 matricielle. Anticancer Res. 2013, 33, 1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA ; Milner, JA Ail et oignons : Leurs propriétés préventives contre le cancer. Cancer Préc. Rés. 2015, 8,181-189. [CrossRef]
- 11. Forte, L. ; Torricelli, P. ; Boanini, E. ; Gazzano, M. ; Rubini, K. ; Fini, M. ; Bigi, A. Propriétés antioxydantes et de réparation osseuse de l'hydroxyapatite fonctionnalisée par la quercétine : étude in vitro de co-culture de cellules ostéoblastes-ostéoclastes-endothéliales. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y. ; Iwasaki, K. ; Mikami, M. ; Yagihashi, A. Distribution de onze précurseurs d'arômes, dérivés de S-Alk(en)yl-L-cystéine, dans sept légumes Allium. Science alimentaire. Technologie. Rés. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. La chimie organosulfurée du genre Allium – Implications pour la chimie organique du soufre. Angew. Chem. Int. Éd. Anglais 1992, 31, 1135-1178. [CrossRef]
- 14. Griffiths, G. ; Trueman, L. ; Crowther, T. ; Thomas, B. ; Smith, B. Oignons-Un bénéfice mondial pour la santé. Phytother. Rés. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S. ; Weston, WJ Développement enzymatique de l'acide pyruvique dans l'oignon comme mesure du piquant. J. Agric. Chimie alimentaire. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, CHAT ; Randle, WM Évaluation du piquant des oignons. Dans Études testées pour l'enseignement en laboratoire ; Karcher, SJ, éd.; Association pour l'enseignement en laboratoire de biologie (ABLE) : New York, NY, États-Unis, 1998 ; Volume 19, pages 177-196.
- 17. Hanelt, P Taxonomie, évolution et histoire. Dans Oignons et cultures connexes, Vol. I. Botanique, Physiologie et Génétique ; Rabinowitch, HD, Brewster, JL, éd.; CRC Press : Boca Raton, FL, États-Unis, 1990 ; p. 1-26.
- 18. Rabinowitch, HD; Currah, L. Science des cultures d'Allium : progrès récents ; CABI Publishing : Wallingford, Royaume-Uni, 2002.
- 19. Mallor, C. ; Carravedo, M. ; Estopanan, G. ; Mallor, F. Caractérisation des ressources génétiques de l'oignon (Allium cepa L.) du centre secondaire espagnol de diversité. Portée. J. Agric. Rés. 2011, 9, 144-155. [CrossRef]
- 20. Ferioli, F. ; D'Antuono, LF Évaluation des composés phénoliques et des sulfoxydes de cystéine dans le matériel génétique local d'oignon et d'échalote d'Italie et d'Ukraine. Genet. Ressource. Récolte Évol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A. ; Barros, L. ; Ferreira, CIFR ; Ntatsi, G. Description morphologique, nutritionnelle et chimique du 'vatikiotiko', une race locale d'oignon de Grèce. Chimie alimentaire. 2015,182, 156-163. [CrossRef]
- 22. Liguori, L. ; Adiletta, G. ; Nazzaro, F. ; Fratianni, F. ; Di Matteo, M. ; Albanese, D. Propriétés biochimiques, antioxydantes et activité antimicrobienne de différentes variétés d'oignons dans la région méditerranéenne. J. Mesures alimentaires. Caract. 2019,13, 1232-1241. [CrossRef]
- 23. Yoo, KS ; Brochet, L. ; Crosby, K. ; Jones, R. ; Leskovar, D. Différences dans le piquant de l'oignon en raison des cultivars, de l'environnement de croissance et de la taille des bulbes. Sci. Hortique. 2006,110, 144-149. [CrossRef]
- 24. Beesk, N. ; Perner, H. ; Schwarz, D. ; George, E. ; Kroh, LW; Rohn, S. Distribution de la quercétine-3, du 4′-O-diglucoside, de la quercétine-4′-O-monoglucoside et de la quercétine dans différentes parties du bulbe d'oignon (Allium cepa L.) influencée par le génotype. Chimie alimentaire. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G. ; Conti, S. ; Villari, G. ; Borrelli, C. ; Melchionna, G. ; Minutolo, M. ; Russo, G. ; Amalfitano, C. Effets du temps de transplantation et de la densité des plantes sur le rendement, la qualité et la teneur en antioxydants de l'oignon (Allium cepa L.) dans le sud de l'Italie. Sci. Hortique. 2014,166, 111-120. [CrossRef]
- 26. Pérez-Gregorio, MR ; Regueiro, J. ; Simal-Gandara, J. ; Rodrigues, AS; Almeida, DPF Augmenter la valeur ajoutée des oignons comme source de flavonoïdes antioxydants : une revue critique. Crit. Rev. Food Sci. Nutr. 2014, 541050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T. ; Schweiggert, RM; Carle, R. Impact de la méthode de culture et de la sélection du cultivar sur les glucides solubles et les principes piquants des oignons (Allium cepa L.). J. Agric. Chimie alimentaire. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I. ; Carbone, V. ; Spagnuolo, C. ; Minasi, P. ; Russo, GL Identification et quantification des flavonoïdes de deux cultivars du sud de l'Italie de Allium cepa L., Tropea (oignon rouge) et Montoro (oignon cuivré), et leur capacité à protéger les érythrocytes humains du stress oxydatif. J. Agric. Chimie alimentaire. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C. ; Esposito, S. ; Carucci, F. ; Frusciante, L. ; Carputo, D. ; Aversano, R. Le génotypage à haut débit de l'oignon révèle la structure de la diversité génétique et des SNP informatifs utiles pour la sélection moléculaire. Mol. Élever. 2019, 39 5. [CrossRef]
- 30. Mercati, F. ; Longo, C. ; Poma, D. ; Araniti, F. ; Lupin, A. ; Mammano, MM; Fiore, MC; Abenavoli, M. ; Sunseri, F Variation génétique d'une tomate italienne à longue conservation (Solanum lycopersicum L.) en utilisant le SSR et les caractères morphologiques du fruit. Genet. Ressource. Récolte Évol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S. ; Mallor, C. ; Garces-Claver, A. ; Mérinos, F. ; Taboada, A. ; Rivera, A. ; Pomar, F. ; Perovic, D. ; Silvar, C. Explorer la diversité génétique et les traits de qualité dans une collection d'oignons (Allium cepa L.) variétés locales du nord-ouest de l’Espagne. Génétique 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C. ; Ioviéno, P. ; Centomani, I. ; Marcotrigiano, AR; Fanelli, V. ; Mimiola, G. ; Summo, C. ; Pavan, S. ; Ricciardi, L. Caractérisation génétique, bio-agronomique et nutritionnelle du chou frisé (Brassica oleracea L. var. accepte-le) diversité dans les Pouilles, dans le sud de l'Italie. Diversité 2018,10 25. [CrossRef]
- 33. Bardaro, N. ; Marcotrigiano, AR; Bracuto, V. ; Mazzeo, R. ; Ricciardi, F. ; Lotti, C. ; Pavan, S. ; Ricciardi, L. Analyse génétique de la résistance à Orobanche crenata (Forsk.) dans un pois (Pisum sativum L.) lignée à faible teneur en strigolactone. J. Pathologie végétale. 2016, 98 671-675.
- 34. Wako, T. ; Tsukazaki, H. ; Yaguchi, S. ; Yamashita, K. ; Ito, S. ; Shigyo, M. Cartographie des loci de caractères quantitatifs pour le temps de montaison dans l'oignon en bottes (Allium fistulosum L.). Euphytique 2016, 209, 537-546. [CrossRef]
- 35. Dacca, N. ; Mukhopadhyay, A. ; Paritosh, K. ; Gupta, V. ; Pental, D. ; Pradhan, AK Identification des SSR géniques et construction d'une carte de liaison basée sur les SSR dans Brassica juncea. Euphytique 2017, 213, 15. [CrossRef]
- 36. Anandhan, S. ; Mote, SR ; Gopal, J. Évaluation de l'identité variétale de l'oignon à l'aide de marqueurs SSR. Semences Sci. Technologie. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K. ; Svoboda, P. ; Ovesna, J. La sélection et la validation d'un ensemble de marqueurs pour la différenciation des cultivars d'oignons de la République tchèque. Tchèque J. Genet. Race végétale. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V. ; Miazzi, MM; Fanelli, V. ; Sabetta, W. ; Montemurro, C. La préservation et la caractérisation de la biodiversité germoplasme de l'olivier des Pouilles. Acta Hortique. 2018,11991-6. [CrossRef]
- 39. Mallor, C. ; Arnedo-Andrés, A. ; Garces-Claver, A. Évaluation de la diversité génétique de l'espagnol Allium cepa variétés locales pour la sélection d'oignons à l'aide de marqueurs microsatellites. Sci. Hortique. 2014,170, 24-31. [CrossRef]
- 40. Rivera, A. ; Mallor, C. ; Garces-Claver, A. ; Garcia-Ulloa, A. ; Pomar, F. ; Silvar, C. Évaluation de la diversité génétique de l'oignon (Allium cepa L.) variétés locales du nord-ouest de l'Espagne et comparaison avec la variabilité européenne. NZJ Culture Hortique. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C. ; Pavan, S. ; Tarente, F. ; Di Rienzo, V. ; Miazzi, MM; Marcotrigiano, AR; Mangini, G. ; Montemurro, C. ; Ricciardi, L. ; Lotti, C. Variation génétique d'une collection mondiale de matériel génétique de pois chiche (Cicer arietinum L.), y compris les accessions italiennes menacées d'érosion génétique. Physiol. Mol. Biol. Plantes 2017, 23, 197-205. [CrossRef]
- 42. Mazzeo, R. ; Morgese, A. ; Sonnante, G. ; Zuluaga, DL; Pavan, S. ; Ricciardi, L. ; Lotti, C. Diversité génétique chez le brocoli-rave (Brassica rapa L. subsp. Sylvestris (L.) Janch.) du sud de l’Italie. Sci. Hortique. 2019, 253, 140-146. [CrossRef]
- 43. Jaksé, M. ; Martin, W. ; McCallum, J. ; Havey, M. Polymorphismes mononucléotidiques, indels et répétitions de séquences simples pour l'identification des cultivars d'oignon. Confiture. Soc. Hortique. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J. ; Thomson, S. ; Pither-Joyce, M. ; Kenel, F. Analyse de la diversité génétique et développement de marqueurs de polymorphisme mononucléotidique dans l'oignon cultivé sur la base de marqueurs de répétition de séquence simple exprimés. Confiture. Soc. Hortique. Sci. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S. ; Pither-Joyce, M. ; Wright, K. ; Chen, L. ; McCallum, J. Développement de marqueurs génomiques robustes de répétition de séquences simples pour l'estimation de la diversité génétique au sein et entre les oignons (Allium cepa L.). Mol. Élever. 2012, 30, 1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Marqueurs microsatellites chez le cerf de Virginie. J. Héréd. 1995, 86 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M. ; Hassanpanah, D. Oignon iranien (Allium cepa L.) réponses des cultivars à la dépression de consanguinité. Appl mondiale. Sci. J 2010,11, 426-428.
- 48. Abdou, R. ; Bakasso, Y. ; Saadou, M. ; Baudoin, JP; Hardy, OJ Diversité génétique des oignons du Niger (Allium cepa L.) évaluée par des marqueurs de répétition de séquence simples (SSR). Acta Hortique. 2016,1143 77-90. [CrossRef]
- 49. Pavan, S. ; Lotti, C. ; Marcotrigiano, AR; Mazzeo, R. ; Bardaro, N. ; Bracuto, V. ; Ricciardi, F. ; Tarente, F. ; D'Agostino, N. ; Schiavulli, A. ; et coll. Un groupe génétique distinct dans le pois chiche cultivé, révélé par la découverte de marqueurs et le génotypage à l'échelle du génome. Génome végétal 2017, 201710. [CrossRef]
- 50. Pavan, S. ; Marcotrigiano, AR; Ciani, E. ; Mazzeo, R. ; Zonno, V. ; Ruggieri, V. ; Lotti, C. ; Ricciardi, L. Génotypage par séquençage d'un melon (Cucumis melo L.) la collecte de matériel génétique provenant d'un centre secondaire de diversité met en évidence les modèles de variation génétique et les caractéristiques génomiques de différents pools génétiques. BMC Génom. 2017, 18 59. [CrossRef]
- 51. Di Rienzo, V. ; Sion, S. ; Tarente, F. ; D'Agostino, N. ; Montemurro, C. ; Fanelli, V. ; Sabetta, W. ; Boucheffa, S. ; Tamendjari, A. ; Pasqualone, A. ; et coll. Flux génétique parmi les populations d'oliviers du bassin méditerranéen. Peer J. 2018, 6. [CrossRef]
- 52. Berger, LD ; McLay, TG Deux protocoles à micro-échelle pour l'isolement de l'ADN à partir de tissus végétaux riches en polysaccharides. J. Plante Rés. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Isolement de l'ADN végétal à partir de tissus frais. Focus 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F. ; Qiaoping, Y. ; Martin, W. ; Zewdie, Y. ; McCallum, J. ; Catanach, A. ; Rutherford, P. ; Évier, KC ; Jenderek, M. ; et coll. Un ensemble unique de 11,008 XNUMX étiquettes de séquence exprimées d’oignons révèle des différences de séquence exprimées et génomiques entre les ordres des asparagales et des poales des monocotylédones. Cellule de plante 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, RH ; Hyun, JY ; Chanson, KH ; Kim, KH ; Kim, JE ; Hur, CG ; Harn, CH Développement de marqueurs pour les tests de pureté génétique de l'oignon à l'aide de SSR Finder. Coréen J. Race. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Une méthode économique pour le marquage fluorescent des fragments PCR. Nat. Biotechnologie. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R. ; Smouse, PE GenAlEx 6.5 : Analyse génétique dans Excel. Logiciels de génétique des populations pour l'enseignement et la recherche : une mise à jour. Bioinformatique 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Cône, ML ; Marshall, TC Réviser la manière dont le programme informatique CERVUS gère les erreurs de génotypage augmente le succès de l'attribution de paternité. Mol. Écol. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M. ; Rosenberg, Caroline du Nord ; Donnelly, P. Cartographie d'association dans des populations structurées. Un m. J. Hum. Genet. 2000, 67 170-181. [CrossRef]
- 60. Evanno, G. ; Regnaut, S. ; Goudet, J. Détection du nombre de grappes d'individus à l'aide du logiciel STRUCTURE : Une étude par simulation. Mol. Écol. 2005,14, 2611-2620. [CrossRef]
- 61. Comte, D. ; VonHoldt, B. STRUCTURE HARVESTER : Un site Web et un programme pour visualiser la sortie STRUCTURE et implémenter la méthode Evanno. Conserver. Genet. Ressource. 2011, 4. [CrossRef]
- 62. Takezaki, N. ; Nei, M. ; Tamura, K. POPTREEW : version Web de POPTREE pour construire des arbres de population à partir de données de fréquence allélique et calculer d'autres quantités. Mol. Biol. Évol. 2014, 31 1622-1624. [CrossRef]
- 63. Kumar, S. ; Stecher, G. ; Li, M. ; Knyaz, C. ; Tamura, K. MEGA X. Analyse génétique évolutive moléculaire sur les plates-formes informatiques. Mol. Biol. Évol. 2018, 35, 1547-1549. [CrossRef]